Yescarta®(Axicabtagene ciloleucel,Axi-cel)自2017年10月18日美国FDA官方批准上市以来,作为全球首个针对既往接受过二线或以上系统性治疗后复发或难治性的大B细胞淋巴瘤(R/R LBCL)成人患者的嵌合抗原受体T细胞(CAR-T)疗法产品[1],开创了淋巴瘤治疗史上的新篇章。今天,Yescarta®迎来了其在全球上市的六周年。在这六年中,随着适应症的不断拓展、受益国家和地区的日益增多、循证医学证据的不断生成以及治疗指南的持续更新,Yescarta®更加稳固地站在了引领淋巴瘤治疗新纪元的前沿,为无数淋巴瘤患者带来了新生的希望,展现了其在淋巴瘤治愈道路上的不可替代性。
一、Yescarta®重燃R/R LBCL患者治愈的新希望
大B细胞淋巴瘤(LBCL)是来源于成熟B细胞的一种恶性淋巴瘤,其中的弥漫性大B细胞淋巴瘤(DLBCL)是最常见的非霍奇金淋巴瘤(NHL)类型,约占所有NHL的25%~50% [2]。经过一线治疗,有约30%~40% 患者复发或难治[3],而既往接受二线或以上系统性治疗后复发或难治性大B细胞淋巴瘤(R/R LBCL)患者往往预后较差,且缺乏有效的治疗手段 ,临床上亟需突破性治疗策略。Yescarta®CAR-T细胞疗法的上市,显著提高了缓解率和长期生存,为R/R LBCL患者带来了治愈的新曙光。
二、Yescarta®推动淋巴瘤治疗模式变革
2.1 Yescarta®多项适应症在全球范围内加速获批
Yescarta®是一种靶向CD19的基因修饰的自体T细胞免疫疗法[4],由美国Kite(吉利德科学旗下公司)研发生产。2017年Yescarta®首次获得美国FDA批准,用于治疗既往接受二线或以上系统性治疗后R/R LBCL成人患者,随后在全球多国加速获批。随着越来越多的临床获益不断被证实,Yescarta®适应症在多国不断扩展,包括治疗线数前移和病种增加(表1)。
表1 国际获批适应症的代表国家
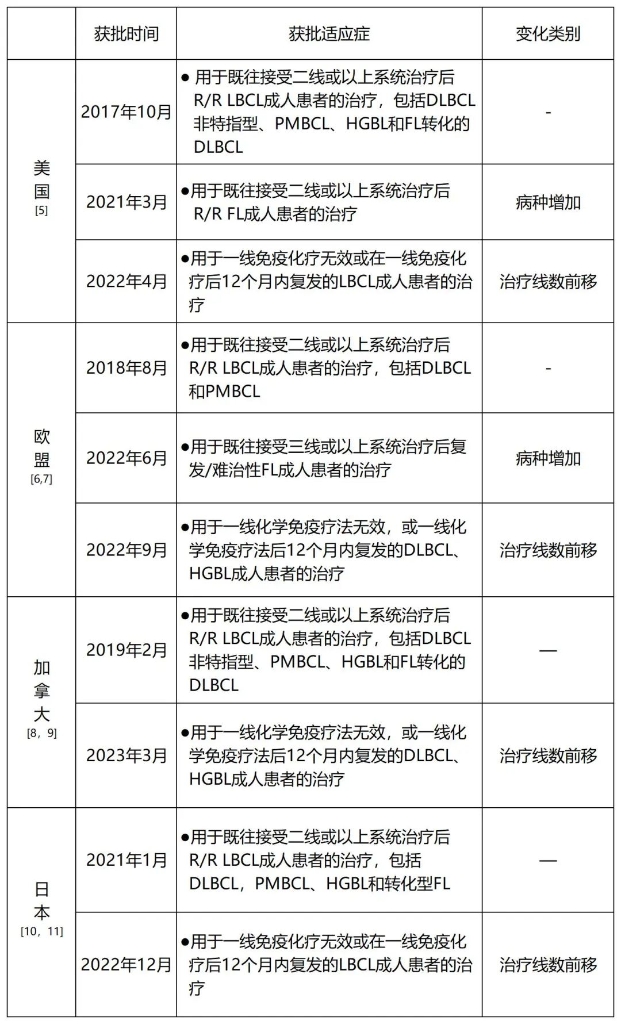
R/R LBCL:复发或难治性大B细胞淋巴瘤;DLBCL: 弥漫性大B细胞淋巴瘤;PMBCL: 原发纵隔大B细胞淋巴瘤;HGBL: 高级别 B 细胞淋巴瘤;FL: 滤泡性淋巴瘤
2. Yescarta®奠定全球淋巴瘤治疗的重要地位
基于显著的生存获益,Yescarta®(Axicabtagene Ciloleucel)获得了NCCN指南(2023.V6)用于原发难治或12个月内复发DLBCL患者二线治疗的I类推荐(表2),展现了Yescarta®在全球淋巴瘤治疗的重要地位。
表2 NCCN指南(2023.V6)推荐

与二线既往标准治疗(SOC,挽救化疗后自体移植)相比,Yescarta®是近30年来首个且目前唯一一个被证明能显著改善R/R LBCL患者总生存期(OS)的治疗产品。2023年6月5日,ASCO年会和《新英格兰医学杂志》(The New England Journal of Medicine,NEJM)分别以口头(Oral)报告形式[13]和全文发布[14]形式同步详细介绍了全球多中心III期随机对照研究ZUMA-7的主要总生存期(OS)分析结果,对于原发难治或12个月内复发的LBCL成人患者,与SOC组相比,Axi-cel治疗组的OS有显著改善 (死亡风险比,0.73;95%置信区间,0.54至0.98;P=0.03),Axi-cel使患者死亡风险降低了27%[14]。中位随访时间为47.2个月时,Axi-cel组未达到中位OS,而SOC组的中位OS为31.1个月。与此同时,Axi-cel组的4年OS率高于SOC组(54.6% vs 46.0%)。
三、奕凯达®塑造中国淋巴瘤治疗新格局
3.1 奕凯达®二线适应症在中国免临床率先获批
奕凯达®(阿基仑赛注射液)是复星凯特从美国Kite引进Yescarta®技术,并获授权在中国进行本地化生产的CAR-T细胞治疗产品。2021年6月23日,奕凯达®在中国获得了国家药品监督管理局(NMPA)的上市批准(用于治疗既往接受二线或以上系统性治疗后R/R LBCL成人患者)。2023年6月21日,其二线新适应症的上市申请也获得了NMPA的正式批准(见表3)。
表3 国内获批适应症
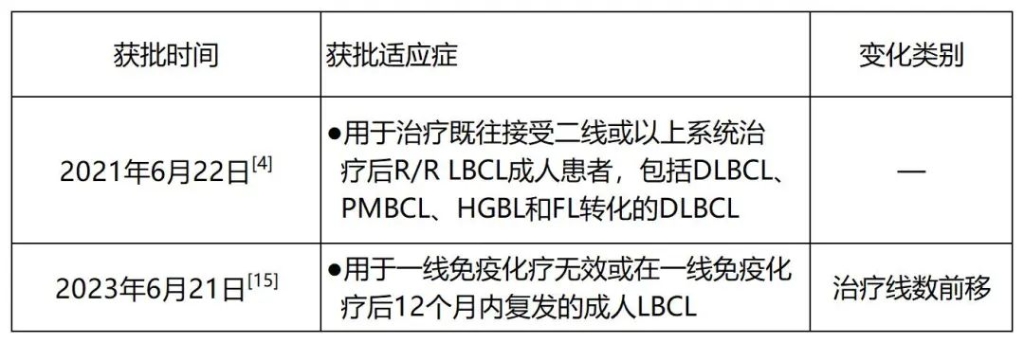
R/R LBCL:复发或难治性大B细胞淋巴瘤;DLBCL: 弥漫性大B细胞淋巴瘤;NOS:非特指型;PMBCL: 原发纵隔大B细胞淋巴瘤;HGBL: 高级别 B 细胞淋巴瘤;FL: 滤泡性淋巴瘤
3.2 奕凯达®奠定中国淋巴瘤治疗的重要地位
基于ZUMA-7研究显著的生存获益,2023年CSCO淋巴瘤诊疗指南将以奕凯达®为代表的 CAR-T疗法升级为I级推荐,用于适合移植,原发难治或12个月内复发的DLBCL患者(表4),这充分展现了奕凯达®在中国R/R LBCL治疗的重要地位。
表4 2023年CSCO指南推荐
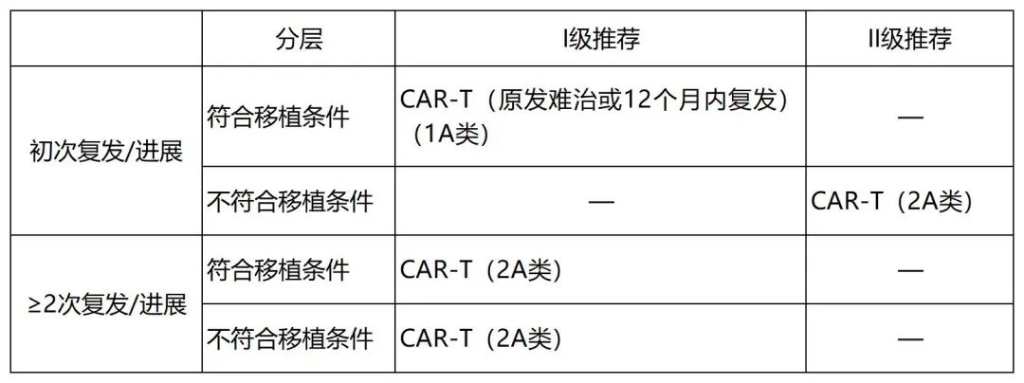
中国多家奕凯达®治疗认证中心收集并分析了接受奕凯达®治疗的R/R NHL受试者的真实世界临床结局。该真实世界研究中期分析成果在2023年6月被EHA和ICML两个顶级国际学术会议以Poster形式接收[17,18]。这是奕凯达®在世界淋巴瘤领域的一次重要亮相,也是中国R/R NHL患者接受商业化CAR-T治疗的首次、大样本、真实世界数据发布。2023年9月21日,奕凯达®对“原发难治或12个月内复发”的R/R LBCL患者的临床数据挖掘结果以commentary的形式也在NEJM上发表,结果提示:对于该类亚裔患者,无论其是否适合ASCT,阿基仑赛治疗均可使患者获益[19]。
相信随着奕凯达®在R/R LBCL患者人群中的临床应用和长期随访以及新适应症的扩展获批,越来越多的中国证据将会生成,从而为奕凯达®更好地治疗中国淋巴瘤患者提供更详实的循证医学证据,为更广泛的中国患者带来长期生存和治愈的希望。
四、Yescarta®不断突破治疗瓶颈,有望成为高危LBCL患者的一线疗法
虽然CAR-T治疗在一线治疗方面目前仍处于探索阶段,但ZUMA-12研究已显示Axi-cel一线治疗高危LBCL患者表现出快速且持久的高缓解率,改善了患者预后[20]。目前,Axi-cel对比SOC治疗一线高危大B细胞淋巴瘤的全球多中心三期随机对照研究ZUMA-23正在开展[21]。Yescarta®不断突破LBCL患者的治疗瓶颈,随着循证医学证据的不断生成,LBCL治疗线数有望前移,重塑LBCL治疗格局。
结语
Yescarta®的成功上市不仅标志着全球淋巴瘤临床治愈时代的到来,更是对淋巴瘤患者渴求治愈的坚定支持。奕凯达®二线新适应症在中国的成功获批,会使更多的中国淋巴瘤患者从中受益。我们期待在未来能为更多淋巴瘤患者带来治愈之光,共同见证CAR-T治疗淋巴瘤的新篇章。
免责声明:本资料为专业医学资料,旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参考;任何处方请参考产品最新详细处方资料。本文件可能包含涉及医学情况、健康及治疗方法的信息。相关信息不得用作诊断或治疗,不能替代专业医学意见。
审批编号:NP-NHL-Axi-Cel-2023.10-18 valid until 2025.10
供稿与审核:临床开发与医学部
参考文献
[1] https://www.fda.gov/media/108458/download
[2] 弥漫性大B细胞淋巴瘤诊疗指南(2022年版).
[3] Zahid U, et al. Curr Hematol Malig Rep. 2017 Jun;12(3):217-226.
[4] 阿基仑赛注射液说明书
[5] Yescarta® (axicabtagene ciloleucel) FDA说明书
[6] Yescarta® (axicabtagene ciloleucel) EMA说明书