ALPK1激动剂的发现与优化
为探索ALPK1激动剂作为癌症免疫治疗的潜力,研究团队首先证实ADP-庚糖能在小鼠和人外周血单个核细胞中诱导ALPK1依赖性炎症反应。随后,他们在包括黑色素瘤和结肠癌在内的多种小鼠癌症模型中,证明了瘤内注射ADP-庚糖能抑制肿瘤生长。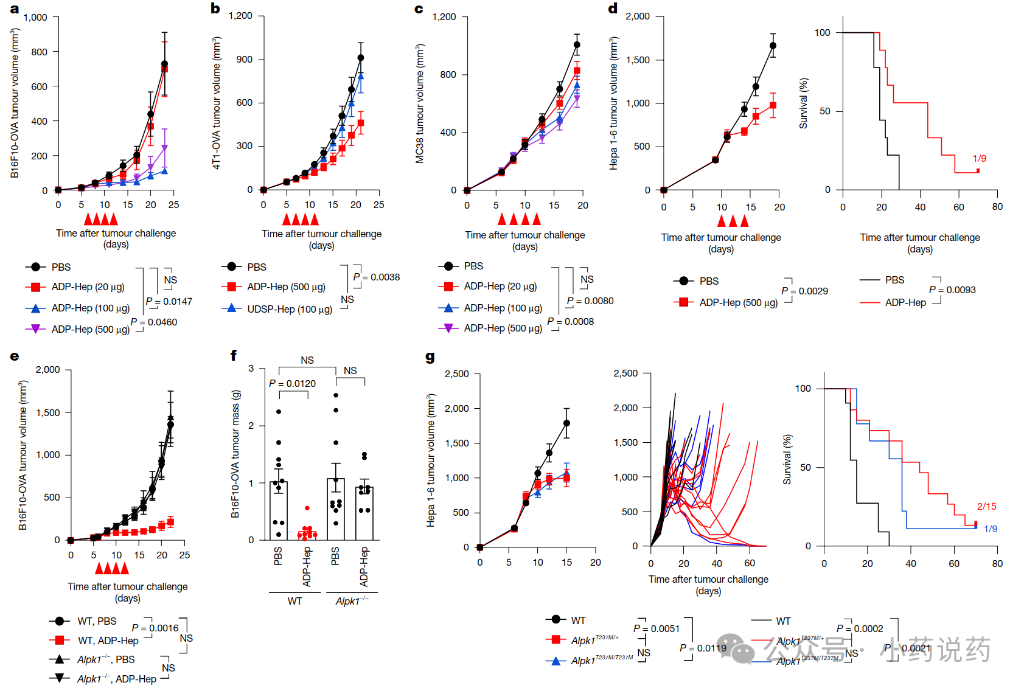
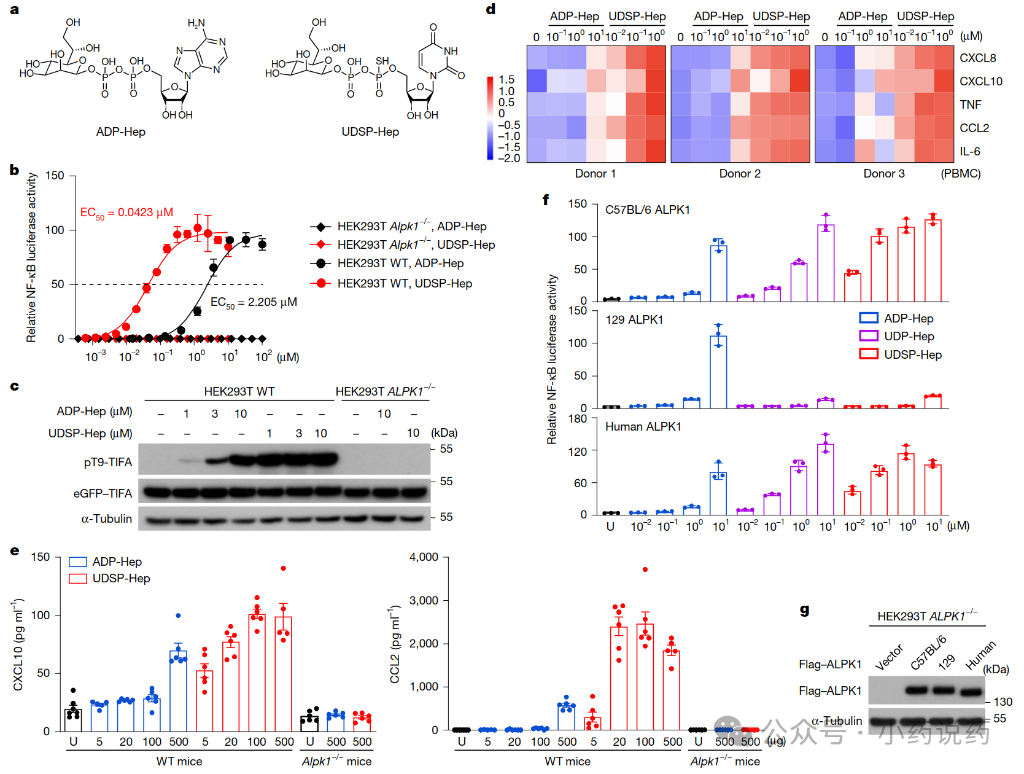
为寻找更强效的ALPK1激动剂,作者合成了ADP-庚糖的类似物。在NF-κB报告基因检测中,将核苷酸部分从ADP改为UDP或CDP能增加效力。对UDP-庚糖进行硫代磷酸酯修饰进一步增强了效力:UDSP-庚糖具有更高的稳定性,并且在细胞中其促炎特性比ADP-庚糖强50倍。当注射到野生型小鼠体内时,与ADP-庚糖相比,UDSP-庚糖也能引发更高水平的炎性细胞因子,而这些效应在缺乏ALPK1的小鼠中消失。
抗癌疗效与协同作用
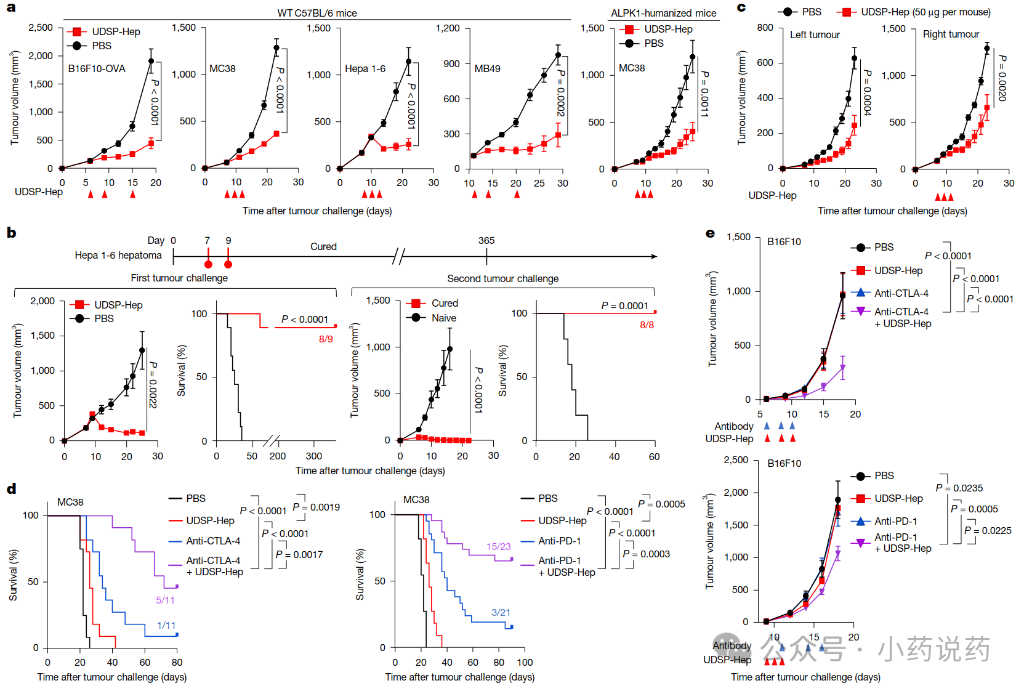
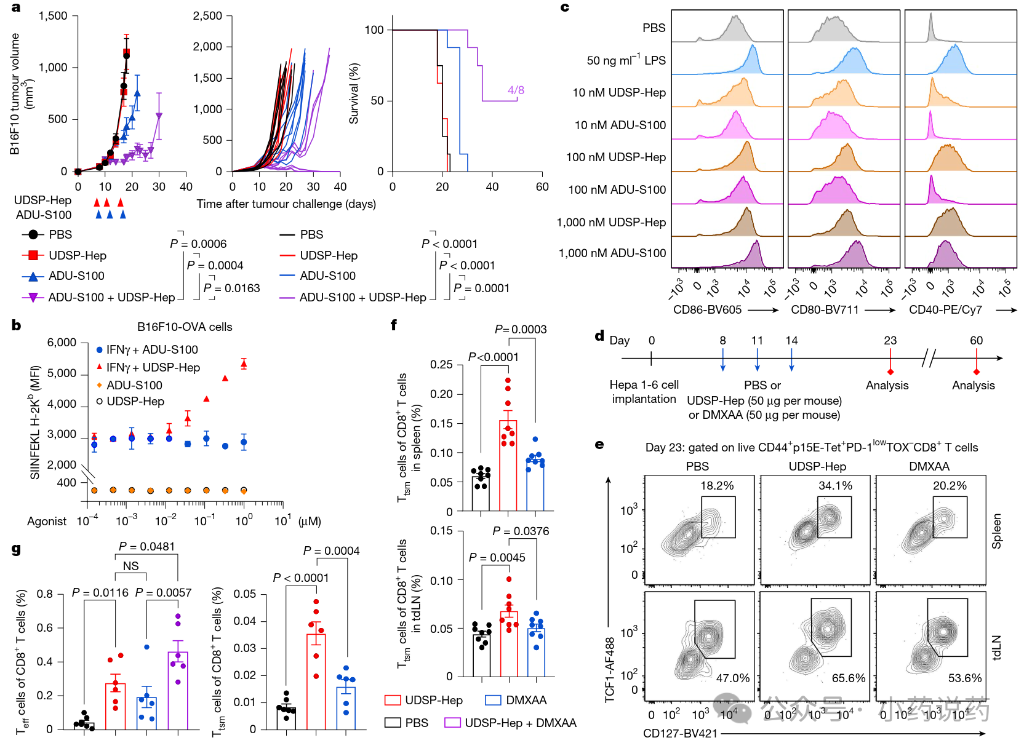
在小鼠肿瘤模型中,UDSP-庚糖比ADP-庚糖更有效,能导致几乎完全的几种肿瘤类型消退,且这种效果依赖于ALPK1。它在ALPK1人源化小鼠中也有效,并且在肿瘤再攻击模型中具有持续活性。此外,UDSP-庚糖与几种检查点抑制剂具有协同作用;例如,当与抗PD-1联合使用时,近70%的结直肠肿瘤小鼠被治愈。
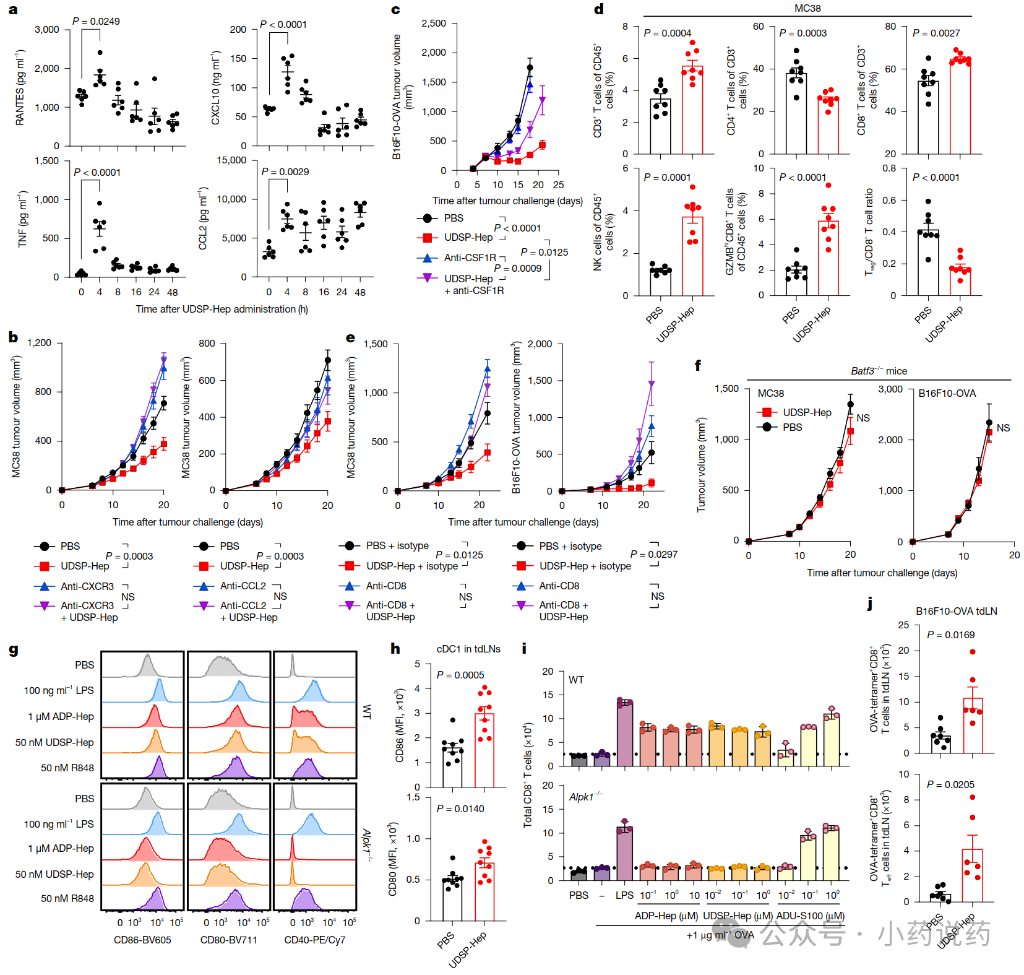
从机制上讲,UDSP-庚肽的抗肿瘤作用需要趋化因子CXCL10和CCL2。它能刺激树突状细胞,并促进肿瘤微环境中CD8⁺ T细胞和自然杀伤细胞水平和活性的增加。
靶点特性与比较优势
ALPK1在免疫细胞系中的表达比TLR7/8/9或STING更广泛,并且每种受体的相应激动剂诱导了不同的细胞因子集合。UDSP-庚糖与STING或TLR激动剂具有协同抗肿瘤效应,进一步表明这些激动剂通过不同通路发挥作用。与STING激动剂相比,UDSP-庚糖还能诱导更高水平的肿瘤特异性记忆T细胞。
结论
这些发现表明,ALPK1是利用先天免疫系统进行癌症治疗的一个新靶点,其特性与其他先天免疫受体形成互补。这为开发新一代癌症免疫疗法提供了新的方向。
参考资料:
1. Innate immune receptor agonist for cancer immunotherapy. Nat Rev Drug Discov. 2026 Jan 12.
2. Agonists for cytosolic bacterial receptor ALPK1 induce antitumour immunity. Nature. 2025 Dec 10.