引言
嵌合抗原受体(CAR)-T细胞疗法已彻底改变了复发/难治性(R/R)B细胞恶性肿瘤和多发性骨髓瘤的治疗格局,通过将活化的T细胞重定向至表达CD19或BCMA的肿瘤细胞来实现治疗。然而,这种方法在急性髓系白血病(AML)这一成人中最常见的急性白血病中尚未获得批准。同时,CAR-T细胞疗法在实体瘤治疗中持续面临重大挑战。在AML中开发CAR-T细胞疗法的主要挑战在于缺乏一个既有效又安全的理想靶抗原,因为AML细胞与健康的造血干细胞和祖细胞共享大多数表面抗原。同时靶向AML细胞和HSPC上的抗原表达可能导致危及生命的靶向/脱肿瘤毒性,例如延长的骨髓消融。此外,AML肿瘤微环境的免疫抑制性质对免疫反应产生不利影响。
-02-
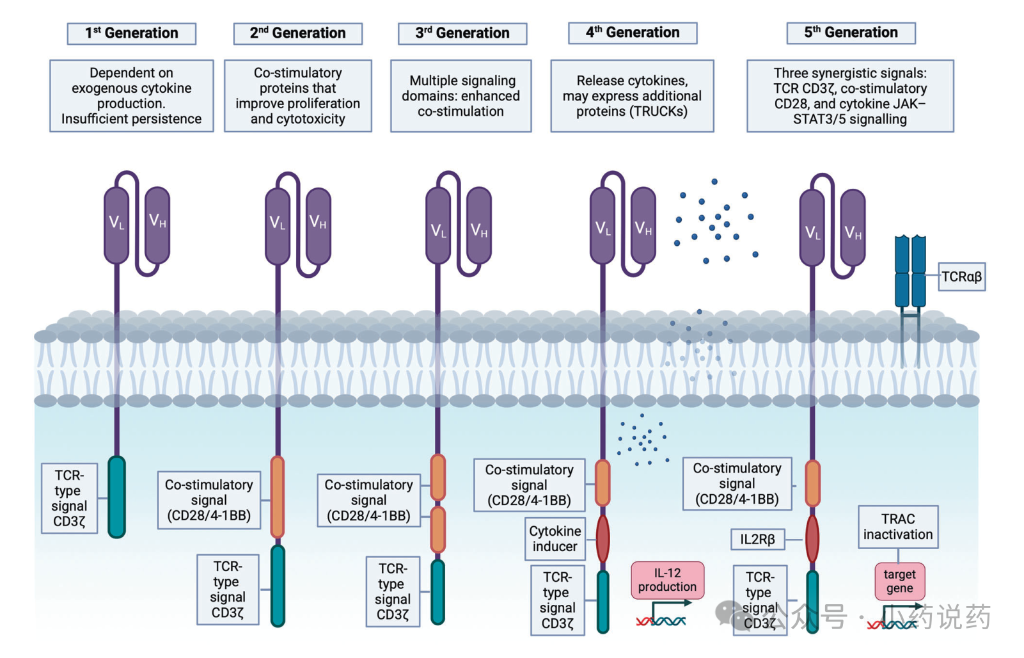
CARs是由一个胞内域、一个锚定跨膜域和一个胞外域组合而成的工程化受体。胞外域是由单链可变片段和铰链组成的配体特异性胞外域。scFv是通过短柔性肽接头连接的免疫球蛋白轻链和重链可变区的融合蛋白。铰链区,也称为间隔区,将结合单元与跨膜域分开。胞内域可能由作为单一实体的CD3ζ的胞内T细胞激活域组成,或者由一个或多个胞内共刺激(或激活)域组成 。虽然scFv提供抗原特异性,但共刺激域是效应T细胞激活的关键。CAR-T细胞根据胞内域分为五代。
第一代CAR-T细胞包含一个源自CD3ζ链的单一片段。这些细胞依赖于外源性细胞因子产生,表现出不充分的持久性和T细胞激活,因此在大多数研究中未能达到预期结果。因此,第一代CARs已被第二代CARs取代,第二代CARs在CARs的胞质尾部包含各种共刺激蛋白受体作为胞内信号域,例如CD28或CD137。这些共刺激蛋白可以增强增殖、细胞毒性并延长持久性。
第三代CARs整合了多个信号域,包括CD28、4-1BB、ICOS和/或OX40。第四代CAR-T细胞,也称为“T细胞重定向用于通用细胞因子介导的杀伤”或“TRUCKs”,被设计用于向肿瘤微环境释放细胞因子。
在下一代CAR-T细胞中,第五代与先前版本的不同之处在于整合了一个额外的膜受体。一种有前景的方法涉及整合IL-2受体信号以实现抗原依赖性JAK/STAT通路激活。这种信号不仅维持CAR-T细胞活性并促进记忆T细胞形成,还能重新激活和刺激更广泛的免疫系统。
目前所有六种已批准的CAR-T细胞构建体都是第二代CARs。
-03-
美国食品药品监督管理局(FDA)已批准六种CAR-T细胞疗法用于治疗各种血液系统恶性肿瘤。Kymriah®是首个获得FDA和欧洲药品管理局(EMA)批准的靶向B细胞抗原CD19的第二代CAR-T细胞疗法,用于治疗儿童和年轻成人ALL。FDA和EMA随后又批准了另外三种靶向CD19抗原的CAR-T细胞疗法:Yescarta®、Tecartus®和Breyanzi®。此外,两种B细胞成熟抗原(BCMA)CAR-T细胞产品已获批用于治疗R/R MM,即Abecma®和Carvykti®。
CAR-T疗法在血液癌症中取得了突破,但其在实体恶性肿瘤中的疗效有限。迄今为止,尚无CAR-T细胞疗法获得FDA或EMA批准用于实体肿瘤。一些临床病例报告表明,针对复发性多灶性胶质母细胞瘤的颅内IL-13Rα靶向CAR治疗有反应,治疗开始后持续了7.5个月。一些关于GD2特异性CAR-T细胞在四名患有H3K27M突变胶质瘤的儿科患者中的证据也有报道,其中三名患者表现出临床和影像学改善。
在实体肿瘤领域,最近更大规模队列的研究显示出显著的抗肿瘤效果。值得注意的是,一项针对37名患者的研究中,一种靶向claudin18.2的CAR被证明可有效治疗胃肠道肿瘤,总缓解率和疾病控制率分别为48.6%和73.0%。此外,一种GD2特异性CAR在27名经过大量预处理的神经母细胞瘤儿童中显示出强劲的结果,总缓解率为63%。
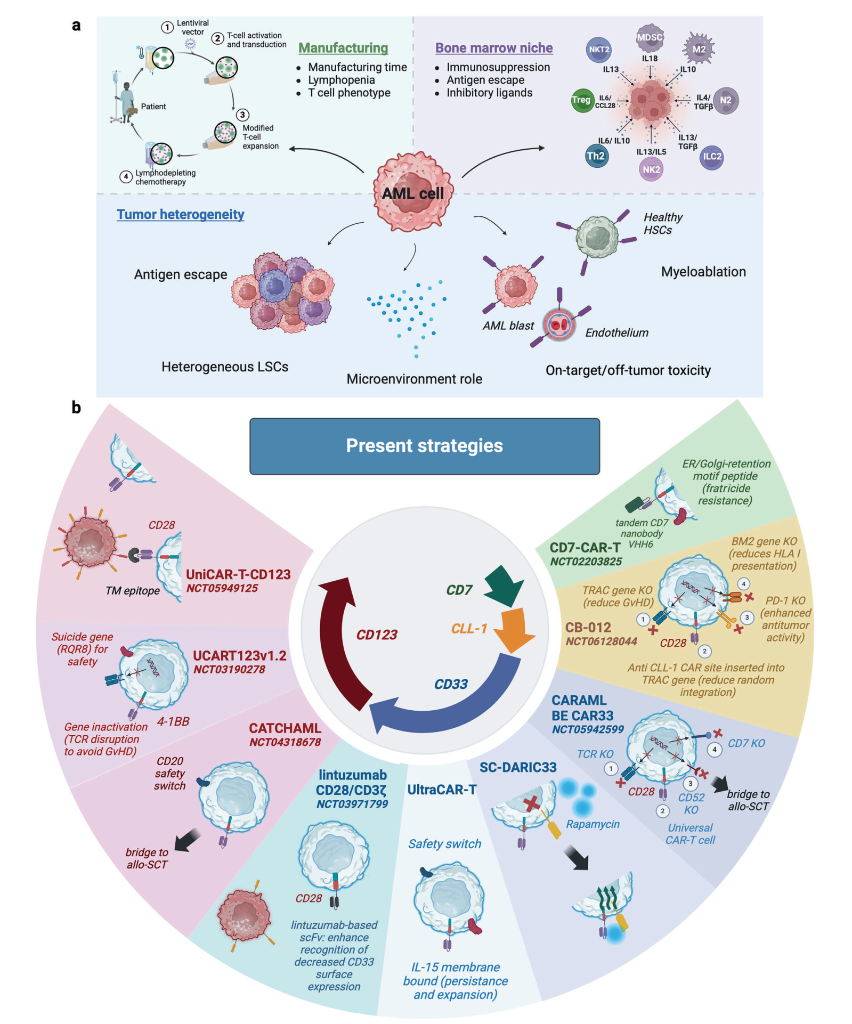
AML的异质性
急性髓系白血病(AML)是一个涵盖多种疾病的广泛类别,每种疾病都有不同的分子和细胞遗传学异常。这种异质性源于影响疾病表现、进展和治疗反应的多种因素。AML的特征是影响关键途径(包括信号转导、表观遗传调控和凋亡)的多种基因突变。这些突变驱动不同的转录程序,导致疾病行为和药物敏感性的变异。此外,染色体易位进一步影响AML的预后和治疗策略。另一个复杂层面来自AML的克隆进化,其中具有不同遗传谱系的亚克隆有助于肿瘤内异质性。
AML被认为反映了正常的造血过程,白血病干细胞(LSCs)通过驱动分化原始细胞的产生来维持疾病。LSCs的特征是低循环或静止、自我更新能力以及与造血干细胞(HSCs)和正常多能造血祖细胞相似的转录或表观遗传特征。LSCs表现出由于静止状态和自我更新潜力而产生的治疗抵抗。
骨髓微环境
AML原始细胞和LSCs呈现出免疫逃逸机制,并重塑骨髓微环境,共同推动疾病进展。首先,在直接与髓系原始细胞相关的内在因素中,NPM1和FLT3的突变与免疫反应的改变有关 。此外,突变型IDH1/2和随后增加的肿瘤代谢物R-2-羟基戊二酸(R2-HG)与AML中调节性T细胞(Tregs)的增加有关。TP53突变也被证明会损害免疫监视。AML中描述的其他内在特征包括HLA分子的下调,导致抗原呈递缺陷;以及细胞因子平衡的改变。
其次,有充分证据表明,高度免疫抑制的骨髓微环境对免疫反应和T细胞适应性产生不利影响。一方面,肿瘤微环境内的代谢产物在免疫抑制中发挥重要作用,限制了免疫疗法的有效性。AML细胞表现出改变的代谢,产生乳酸、腺苷和犬尿氨酸,这些物质促成了一个阻碍CAR-T细胞功能的有害微环境。升高的乳酸水平会导致TME酸化,抑制T细胞激活和增殖。此外,腺苷结合CAR-T细胞上的受体,导致免疫抑制和耗竭。同样,犬尿氨酸也会抑制T细胞功能并促进免疫抑制环境。
另一方面,与健康个体相比,AML的特征是浸润骨髓的T细胞数量增加。这些T细胞表现出免疫抑制性和激活共受体表达频率的增加,尤其是在R/R AML中。这包括PD-1、OX40、TIM3和LAG3的表达。总体而言,T细胞在这种背景下表现出不足的效力、持久性和功能。这种T细胞耗竭通常不仅以高表达抑制性受体为特征,还与广泛的转录和表观遗传改变、细胞因子产生缺陷、趋化因子表达增加以及从T细胞向NK样T细胞表型的转变有关。
第三,除了与髓系原始细胞直接相关的内在因素外,M2巨噬细胞的扩增也被证明可增强AML免疫逃逸。此外,免疫突触功能差和NK细胞功能受损已被确定为参与此过程的机制。最后,考虑骨髓结构在细胞成分之外可能发挥的作用也很重要。骨髓血管重塑可能通过减少细胞迁移和诱导缺氧来阻碍抗AML免疫反应。
靶抗原
确定AML中CAR-T细胞疗法的合适靶点至关重要。一个合适的靶点应该是AML细胞表面表达的、不受HLA限制的抗原/蛋白,且表达水平较高。理想情况下,该抗原也应在LSCs上表达,以确保彻底根除疾病并最大限度地减少早期复发。重要的是,它必须在健康组织中不存在,以防止可能致命的靶向/脱肿瘤毒性。迄今为止,尚未确定AML中CAR-T细胞疗法的最佳靶点。AML新抗原相对不常见,且已知主要是胞内的,需要HLA呈递。在当前的临床实践中,CD33和CD123是CAR-T细胞工程中最常用的分子。
CD123,也称为IL-3受体的α链(IL-3Rα),是一种在AML中高表达的膜蛋白。CD123也存在于其他髓系恶性肿瘤中。CD123参与JAK、MAPK和PI3K/AKT信号通路,这些通路调节细胞增殖和分化。CD123的过表达已在高达95%的LSCs和AML原始细胞中被识别。关于靶向/脱肿瘤毒性,其HSCs上的表达存在争议。一个重要的担忧是潜在的髓外毒性,因为CD123在内皮细胞上表达,可能导致毛细血管渗漏综合征。几种未偶联的单克隆抗体(mAbs),包括CD123导向的mAbs CSL360和CSL362(talacotuzumab),在治疗R/R AML中显示出有限的疗效。因此,目前的策略主要包括使用毒素偶联构建体或双特异性T细胞衔接器(BiTEs)。
CD33是一种由唾液酸残基刺激的跨膜受体,在大约85%的AML病例中表达。已知它在超过85%的LSCs中存在,在HSCs中表达相对较低。人源化抗CD33抗体药物偶联物吉妥珠单抗奥佐米星已获EMA和FDA批准,与强化化疗联合用于初治AML的一线治疗。报告的主要毒性是持续性血小板减少症和肝窦阻塞综合征(VOD)。与抗CD123未偶联分子报告的证据一致,针对CD33的mAbs和抗体药物偶联物(如林妥珠单抗、SGN-CD33A和IMGN779)迄今为止未能显示出相关的抗白血病活性。值得注意的是,几种CD33×CD3 BiTEs在针对R/R AML的临床试验中显示出有希望的结果和可接受的毒性特征。
临床试验中的CD123-CAR-T细胞
2020年,一个德国研究小组报告了靶向CD123的UniCAR-T-CD123的临床前疗效,这是一种双组分、可快速切换的第二代CAR-T。该构建体携带一个CD28共刺激域,其本身除了一个名为靶向模块的可溶性衔接器外,不识别任何表面抗原 。TM通过静脉注射给药,并赋予对所选抗原的特异性。
该策略目前正在一项针对R/R AML的Ia期试验中进行研究,早期结果令人鼓舞,毒性特征可接受。事实上,该试验被修改为包括延长的TM给药方案。迄今为止,19名经过大量预处理的患者已接受UniCAR-T-CD123治疗,包括12名曾接受过异基因造血干细胞移植的患者 。细胞因子释放综合征(CRS)在12名患者中观察到,主要为1级或2级。未观察到延长的骨髓抑制,因此不需要救援性异基因造血干细胞移植。R/R AML人群的总缓解率(ORR)为53%。
同一研究小组开发了世界上第一个CRISPR工程化的可切换同种异体CAR-T,旨在避免移植物抗宿主病(GvHD)和细胞排斥。该试验目前正在进行中。
临床试验中的CD33-CAR-T细胞
一种包含林妥珠单抗-CD28/CD3的第二代CD33导向的CAR构建体,在针对儿童、青少年和年轻成人R/R AML的I/II期剂量递增中期分析中显示出有希望的结果。该构建体包括一个源自林妥珠单抗的靶向基序,与CD28/CD3连接。
共有24名受试者入组试验,其中12名曾接受过异基因造血干细胞移植。CD33-CAR-T产品成功为23名患者制造,随后输注给19名患者,主要原因是疾病进展。4名患者经历了3级或4级CRS,但得到成功管理。在达到最高剂量水平的患者中报告了反应。
总的来说,尽管在理解AML异质性和免疫逃逸方面取得了重大进展,但仍需要进一步的研究来优化CAR-T细胞策略并克服AML治疗的内在挑战 。将多靶点方法、改进的制造技术和更深入地了解BM微环境相结合,最终可能增强CAR-T细胞在AML中的治疗潜力。
参考资料:
CAR-T cell therapy for cancer: current challenges and future directions. Signal Transduct Target Ther. 2025 Jul 4;10(1):210